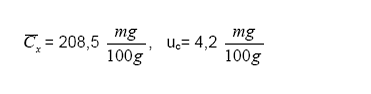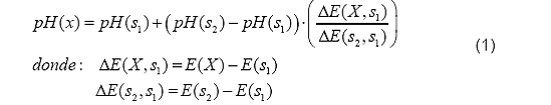
10.
BIBLIOGRAFÍA
- ILAC-P14:12/2010
ILAC Policy for Uncertainty in Calibration
- OIML/V2
Vocabulario Internacional de Términos Básicos de Metrología, Segunda edición
2009.
- Guía
BIPM/ISO para la expresión de la incertidumbre en mediciones (GUM).
- Norma
INTE-ISO/IEC 17025:2005 Requisitos generales para la competencia de laboratorios
de ensayo y calibración.
10.
ANEXOS: EJEMPLOS DE ESTIMACIÓN DE INCERTIDUMBRE:
Se
les recuerda que las estimaciones de incertidumbre deben realizarse conforme a
Ejemplo
1: Determinación del valor de la actividad del ión hidronio en una muestra incógnita:
Se
desea determinar el valor de la actividad del ion hidronio, en una muestra incógnita,
realizando la curva de pH con dos disoluciones amortiguadoras de 4,00 ± 0,02 y
7,00 ± 0,02, a
Modelo
matemático
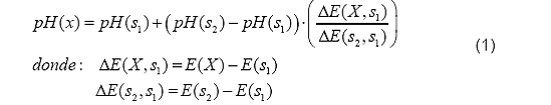
Donde:
pH(s1)
= valor de pH de la disolución amortiguadora 1
pH(s2)
= valor de pH de la disolución amortiguadora 2
E(X)
= potencial en mV, de la muestra
E(s1)
= potencial en mV, de la disolución amortiguadora 1
E(s2)
= potencial en mV, de la disolución amortiguadora 2
Resultados
experimentales
pH(s1)=
4,00 E(s1)=167,9 mV
pH(s2)=
7,00 E(s2)=- 4,0 mV
E(X)=
158,2 mV
A
partir de los datos anteriores determinó que el valor de la actividad de ion
hidronio en la muestra es de: pH(X) = 4,169
Las
variables de entrada pueden ser observadas en la figura 1.
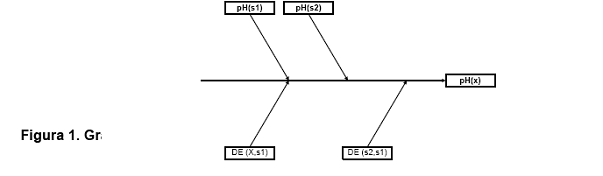 Para
determinar la incertidumbre estándar de la determinación, utilizamos la
siguiente fórmula:
Para
determinar la incertidumbre estándar de la determinación, utilizamos la
siguiente fórmula:
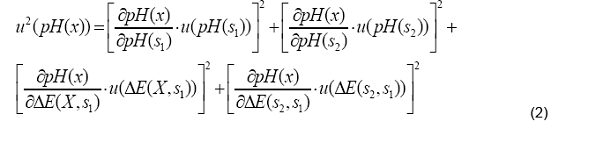 Donde
son los coeficientes de sensibilidad
Donde
son los coeficientes de sensibilidad
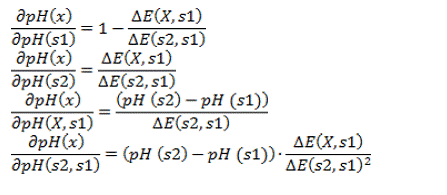
Por
lo tanto, al sustituir los resultados experimentales en las ecuaciones de
coeficientes de sensibilidad, tenemos:

Para
determinar la incertidumbre estándar de cada variable, debo considerar la
información suministrada por el fabricante o determinada experimentalmente, en
nuestro caso específico solamente consideramos al fabricante. No existe
información suficiente, que me indique que la tolerancia indicada por el
fabricante de las soluciones amortiguadoras y la tolerancia del potenciómetro,
tienen alguna distribución específica, por lo tanto considero que las mismas
tienen distribución rectangular.
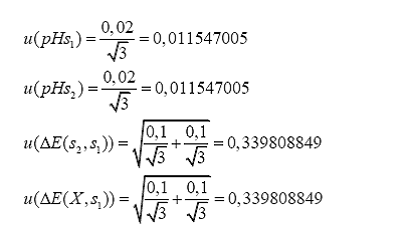
Finalmente,
sustituyo y obtengo la incertidumbre estándar

Ejemplo
2. Cálculo de incertidumbre asociado a las contribuciones sobre una magnitud
obtenida por medición directa.
Determinación
de la incertidumbre combinada asociada a una determinación de masa en una
balanza analítica digital con resolución de 0,5 mg.
Indicación
del instrumento
m
=
Contribuciones
a la incertidumbre:
a.
incertidumbre estándar por calibración:
Tolerancia
por calibración (linealidad) =
Distribución
= rectangular
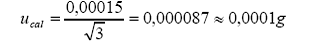
b.
incertidumbre estándar por lectura en escala digital: Tolerancia
por lectura (resolución digital) =0,0005 g
Distribución
= rectangular
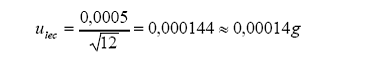
Cálculo
de incertidumbre:
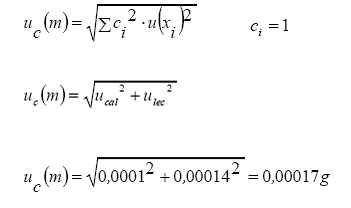
Reporte
de resultado
![]()
Ejemplo
3: Cálculo de incertidumbre asociado a las contribuciones sobre una magnitud
obtenida por medición directa.
Ejemplo:
Determinación
de la incertidumbre combinada asociada a la operación de medición y vertido de
un volumen de 10,0 mL utilizando una pipeta graduada con capacidad máxima de
20,0 mL.
![]()
Contribuciones
a la incertidumbre:
a.
Incertidumbre estándar por tolerancia del fabricante a 20 °C:
Tolerancia
por 0,03 mL±calibración
=
Distribución
= triangular
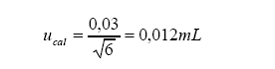
b.
incertidumbre estándar por lectura de la escala graduada:
La
incertidumbre asociada al proceso de lectura de la escala de una pipeta graduada
se determina a partir de la resolución de la escala graduada.
Resolución
de la escala:
Mínima
división de escala = 0,02 mL
Factor
de ojo = 2
Distribución
= rectangular
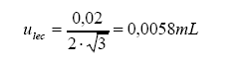
c.
Incertidumbre estándar por diferencia entre la temperatura de calibración (
Variación
máxima de temperatura alrededor de
Coeficiente
de expansión 10-4 °C-1×térmica
del agua = 2,1
Distribución
= rectangular
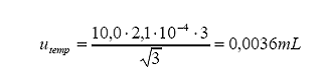
d.
Repetibilidad:
s=0,025
(desviación estándar a partir de 7 réplicas)
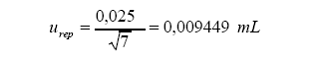
Cálculo
de incertidumbre combinada:
![]()
Reporte
de resultado:
Vpipeta
= 10,00 mL, uc = 0,017 mL
Ejemplo
4: Cálculo de la incertidumbre asociada a una cantidad obtenida mediante una
operación fundamental tipo multiplicación y/o división.
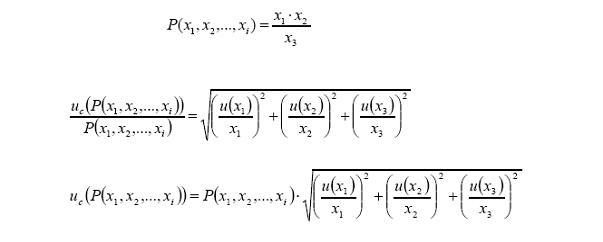
Ejemplo:
Determinación
de la incertidumbre asociada a la concentración de una disolución de KCl
obtenida al disolver

Contribuciones
a la incertidumbre:
a.
Incertidumbre estándar asociada a la balanza analítica.
incertidumbre
estándar por calibración:
Tolerancia
por calibración (linealidad) =
Distribución
= rectangular
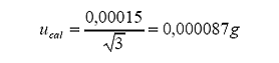
Incertidumbre
estándar por lectura en escala digital: Incertidumbre por lectura (resolución
digital)
Distribución
= rectangular
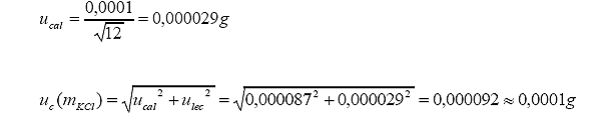
b.
Incertidumbre estándar asociada al peso molecular.


c.
Incertidumbre estándar asociada a la pureza.
Tolerancia
del 0,5 %)±fabricante
= 0,005 (98,0
Distribución
= rectangular
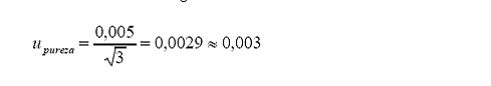
d.
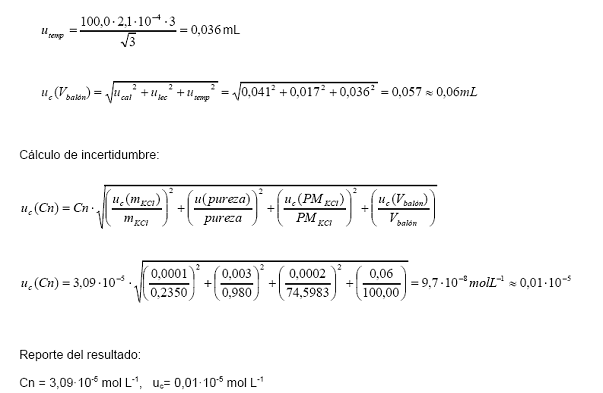
Incertidumbre estándar asociada al balón aforado.
Incertidumbre
estándar por calibración del fabricante a 20 °C:
Tolerancia
por 0,1 mL±calibración
=
Distribución
= triangular
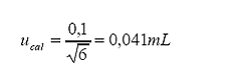
incertidumbre
estándar por lectura de la marca de aforo:
Reproducibilidad
= 0,035 (desviación estándar a partir de 5 réplicas)
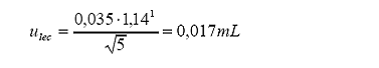
1
estadístico
t para 4 grados de libertad y 68% de confianza.
Incertidumbre
estándar por diferencia entre la temperatura de calibración (
Variación
máxima de temperatura alrededor de
Coeficiente
de expansión 10-4 °C-1×térmica
del agua = 2,1
Distribución
= rectangular
Ejemplo
6: Determinación de la concentración promedio de cierto componente x en un
alimento mediante la técnica de espectrofotometría ultravioleta. Luego de
seguir el procedimiento indicado, el cálculo de la concentración del
componente x se obtiene según la fórmula:
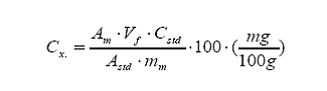
En
términos de la absorbancia, masa y volumen final de la muestra.
Los
resultados obtenidos para tres muestras del alimento se indican en la siguiente
tabla:
|
#
muestra |
mm/g
|
Am
|
|
1
|
25,2356
|
0,385
|
|
2
|
27,4578
|
0,421
|
|
3
|
26,1167
|
0,393
|
1.
Cálculo de concentración y análisis de incertidumbre para la muestra #1:


2.
Cálculo e incertidumbre de la concentración promedio del componente x:
Un
procedimiento de cálculo similar aplicado a las otras dos muestras permite
obtener los resultados resumidos en la siguiente tabla:
|
#
muestra |
Cx
/gmg100
|
uc(Cx)
|
|
1
|
209,1
|
6,7
|
|
2
|
210,2
|
6,7
|
|
3
|
206,2
|
6,6
|
De
donde se obtiene el valor de la concentración promedio con su respectiva
incertidumbre estándar:
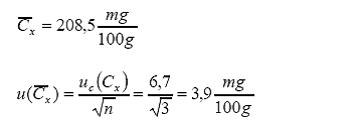
Para
completar el cálculo de incertidumbre del valor promedio se debe de tomar en
cuenta la contribución por repetibilidad. Esta se calcula en términos del desvío
estándar de las réplicas respecto del valor promedio:
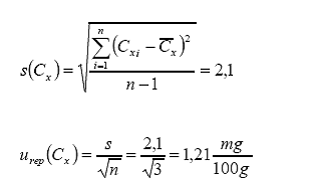
Ahora
el cálculo de la incertidumbre estándar combinada total del valor promedio será
ahora:
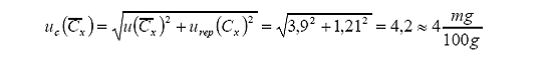
Reporte
de resultado: